-
Produits
-
Instruments de laboratoire
Systèmes de titrage Beverage Analysers
-
Appareils de mesure et sondes
Standards d'étalonnage Capteurs Radiometer
- Chimies, réactifs et étalons
-
Analyseurs en ligne
Analyseurs d'ammonium Analyseurs de chlore
- CL17sc
- CL10 sc Ampérométrique
- 9184 sc Ampérométrique
- Analyseur colorimétrique de chlore Cl17sc Ultra Low Range
Analyseurs de phosphates- NP6000sc
- Système FX610/FX620
- Système Filtrax
- Phosphax sc
- Phosphax sc basse valeur
- 5500 sc
- NP6000sc Chemistry/Reagents
- Phosphax Sigma
Analyseurs de la série EZ- Fer
- Aluminium
- Manganèse
- Phosphate
- Chlorure
- Cyanure
- Fluorure
- Sulfate
- Sulfure
- Arsenic
- Chrome
- Cuivre
- Nickel
- Zinc
- Ammonium
- Azote total
- Phosphore total
- Phénol
- Acides gras volatils
- Alcalinité
- ATP
- Dureté
- Toxicité
- Préconditionnement d'échantillon
- Bore
- Couleur
- Nitrate
- Nitrite
- Silice
- Peroxyde d'hydrogène
- EZ Series Reagents
- EZ Series Accessoires
- EZ sc Series Additional Analyzers
- Série EZ sc - Matières inorganiques
- Série EZ sc - Métaux
- Série EZ sc - Nutriments
-
Contrôleurs et capteurs en ligne
Transmetteurs numériques Contrôleurs (analogiques) Ammonium Sensors Capteur de surveillance du sulfure d'hydrogèneMulti-paramètre Capteurs pH et ORP
- 1200-S Redox
- 1200-S pH
- 12mm pH/Redox
- 8362 sc ultra pure
- Combinaison pH/Redox
- LCP Redox
- LCP pH/Redox
- Redox différentiel numérique
- pH différentiel
- pH différentiel numérique
Huile dans l'eau Matières organiques Niveau de boue Solides en suspension Conditionnement d'échantillon -
Systèmes de laboratoires automatisés
Robot Systems
- Échantillonnage
- Multiparameter Online Panels
- Claros Water Intelligence System
- Kits de test et bandelettes
-
Microbiologie
Instruments Installation de laboratoireKits Support préparéSupport déshydraté Accessoires et produits chimiques
-
Fournitures et équipements de laboratoire
AppareilInstruments Consommables de laboratoire générauxLivres et matériels de référenceVerrerie/plastique
- Electrochimie
-
Instruments de laboratoire
- PARAMETRES
-
Solutions logicielles
-
Water Intelligence System Claros pour la qualité de l'eau
Principes fondamentaux du produit Process Management
- Solutions pour:
- Elimination du DBO/DCO
- Nitrification/dénitrification
- Elimination du phosphore
- Gestion des boues
Data Management- Solutions pour:
- Collecte
- Visualisation et analyse
- Création de rapports
- Exactitude des données
Instrument Management- Solutions pour:
- Maintenance
- Dépannage
- Accès à distance
- Comparaison de laboratoire et de procédés
-
Water Intelligence System Claros pour la qualité de l'eau
- Industries
- Service
- Actualités et événements
France
Choisir votre pays ou région:
Europe
Americas
Asia - Australasia
- Australia
- Mainland China
- India
- Indonesia
- Japan
- Malaysia
- New Zealand
- Philippines
- Singapore
- South Korea
- Thailand (Thai)
- Taiwan
- Vietnam
Middle East - Africa
Dureté (totale, Ca et Mg)
Qu'est-ce que la dureté ?
La dureté est une mesure de la capacité d'absorption du savon dans l'eau. A l'origine, ce terme exprimait la difficulté à laver des vêtements à l'eau, à savoir si cela était plus ou moins « dur » à faire. Lorsque le savon se mélange à de l'eau dure, les minéraux se combinent au savon et forment un précipité solide. Cela réduit l'efficacité de lavage du savon et produit de l'écume. A mesure que l'on ajoute du savon, des matières solides continuent de se former jusqu'à épuisement des minéraux. Lorsqu'il n'y a plus de minéraux, le savon produit une mousse et agit à la manière d'un agent de nettoyage.
Les minéraux qui réagissent avec le savon correspondent aux cations de métaux polyvalents tels que le calcium, le magnésium, le fer, le manganèse et le zinc. La concentration de calcium et de magnésium dans les eaux naturelles dépasse généralement de loin celle de tout autre cation polyvalent. C'est pourquoi on considère que la dureté est la concentration d'ions calcium et magnésium dans l'eau.
Dureté carbonatée et non carbonatée
La dureté peut être soit carbonatée soit non carbonatée. La dureté carbonatée fait référence au bicarbonate de calcium et de magnésium. On parle parfois de dureté temporaire, car elle peut être éliminée ou réduite par ébullition. Lorsqu'ils sont chauffés, ces bicarbonates forment un précipité de carbonate solide. Il s'agit de la principale cause de formation de tartre dans les chauffe-eau et les chaudières. La dureté non carbonatée est principalement due aux nitrates, aux chlorures et aux sulfates de calcium et de magnésium. La dureté non carbonatée est parfois appelée dureté permanente.
Pour calculer le niveau de dureté carbonatée par rapport à la dureté non carbonatée, il suffit de mesurer l'alcalinité. Si l'alcalinité est supérieure ou égale à la dureté, toute la dureté est carbonatée. Une dureté excessive est une dureté non carbonatée. La dureté est généralement exprimée en mg/L pour CaCO3. L'alcalinité étant également rapportée pour CaCO3, les résultats des deux tests peuvent être comparés immédiatement. La dureté totale est la somme de tous les sels de calcium et de magnésium, carbonatés et non carbonatés, présents dans l'eau.
Pourquoi mesurer la dureté ?
En général, l'eau dure forme des dépôts solides composés principalement de sels de calcium et de magnésium et peut endommager le matériel, tandis que l'eau douce peut être corrosive. Par conséquent, il est important de mesurer et de connaître les niveaux de dureté de l'eau de traitement afin de maintenir le fragile équilibre entre entartrage et corrosivité.
Bien qu'une certaine dureté soit acceptable dans quelques applications relatives à la qualité de l'eau, d'autres nécessitent néanmoins une dureté nulle pour éviter le tartre et les dommages au niveau du matériel. C'est pourquoi il est souvent nécessaire d'adoucir l'eau par précipitation ou échange d'ions afin d'éliminer la dureté. Pour optimiser ces processus, il est parfois important de surveiller séparément les niveaux de calcium et de magnésium, ainsi que la dureté totale.
En outre, le magnésium peut interférer avec d'autres tests de la qualité de l'eau, par exemple la méthode au salicylate pour la détermination de l'azote ammoniacal. Pour en savoir plus sur l'azote et l'ammoniac, consultez les pages Paramètres connexes.
Chez Hach®, trouvez l'équipement, les réactifs, les ressources, les formations et les logiciels dont vous avez besoin pour surveiller et gérer avec succès la dureté de l'eau dans votre application spécifique.
Produits associés pour mesurer la dureté
L'analyseur de dureté SP510 de Hach surveille en continu les réseaux de distribution d'eau et déclenche une alarme lorsque la dureté totale dépasse une limite préétablie.
En savoir plusAnalyseurs de dureté de la série EZ
Les analyseurs en ligne de la série EZ fournissent plusieurs options pour surveiller la dureté totale et la dureté calcique de l'eau.
En savoir plusSL1000 - Analyseur parallèle portable PPA - Colorimètre portable avec USB
L'analyseur parallèle portable (PPA) Hach SL1000 réalise les mêmes tests avec moitié moins d'étapes manuelles.
En savoir plusLes titrateurs numériques de Hach utilisent un appareil de distribution de grande précision, ainsi que des cartouches de solution titrée remplaçables, permettant d'obtenir des résultats très précis sur le terrain ou en laboratoire.
En savoir plusKit de titrage AT1000, dureté totale, Ca et Mg (ISE)
Tout ce dont vous avez besoin pour titrer la dureté totale (Ca et Mg) est disponible dans un seul kit.
En savoir plusKit de titrage AT1000, dureté totale (couleur)
Tout ce dont vous avez besoin pour titrer la dureté totale (couleur) est disponible dans un seul kit.
En savoir plusProduits chimiques haute qualité Hach sur bandelette de test facile à utiliser. Il vous suffit de plonger la bandelette dans l'échantillon et de la comparer avec les couleurs imprimées sur le flacon pour déterminer une valeur. Les bandelettes de test sont précises, portables et économiques.
En savoir plus
Quels sont les procédés qui nécessitent une surveillance de la dureté ?
Traitement de l'eau potable
Une eau traitée excessivement dure libérée dans le réseau de distribution peut provoquer un entartrage, mais une eau trop douce peut entraîner la corrosion des tuyaux. Du plomb et du cuivre peuvent alors pénétrer dans l'eau, ce qui va à l'encontre de la réglementation en vigueur.

Eaux usées
Pendant la digestion des boues, surveillez la dureté pour optimiser l'efficacité. La biodégradation du savon et l'absorption d'oxygène par les boues activées sont affectées par des concentrations de dureté élevées.

Test de l'eau des piscines et des spas
Une eau trop dure peut provoquer un entartrage, c'est-à-dire des dépôts de carbonate de calcium. Quant à l'eau douce, elle corrode les tuyaux et les surfaces de la piscine, qui contiennent du calcium (notamment l'enduit) et d'autres minéraux.

Secteur de l'électricité
La dureté de l'eau peut provoquer un entartrage dans les chauffe-eau et les tubes de chaudière. C'est pourquoi il est essentiel de surveiller et d'éliminer tous les sels, en particulier ceux qui sont à l'origine de la dureté.

Fabrication de produits chimiques
Surveillez la teneur en minéraux de l'eau entrante afin d'ajuster correctement la qualité de l'eau produite et les facteurs sensoriels. Surveillez les performances des systèmes d'adoucissement de l'eau pour éviter l'entartrage et évaluez la charge sur les systèmes d'osmose inverse. La surveillance continue de l'eau de chaudière et de refroidissement (sortant du condenseur) permet de détecter des niveaux de dureté infimes et fluctuants risquant, au fil du temps, d'entartrer les canalisations, les condenseurs et les sécheurs. Cela permet également aux opérateurs de gérer les niveaux de dureté afin d'éviter les dommages et les pertes de chiffre d'affaires liés aux temps d'arrêt.

Secteur agroalimentaire
Surveillez et gérez la dureté totale pour optimiser l'alimentation en eau des chaudières et des tours de refroidissement. Cela permet de diminuer l'utilisation de produits chimiques, d'empêcher la corrosion et l'entartrage et de protéger l'équipement de l'usine.

Industrie minière
L'eau est essentielle dans le secteur de la métallurgie et de l'exploitation minière, mais cette industrie est rarement la seule consommatrice d'eau à proximité des sites d'extraction ou de traitement. En surveillant et en traitant l'eau de source, les compagnies minières s'assurent non seulement de respecter leurs propres normes de qualité, mais elles peuvent dans le même temps contribuer à la bonne santé des communautés, des ressources agricoles ainsi que des écosystèmes, de la faune et de la flore. Qu'elle provienne de nappes phréatiques ou de précipitations, d'océans ou de lacs, de fleuves ou de ruisseaux, par le biais d'un réseau commercial ou municipal, l'eau utilisée dans l'exploitation minière est interconnectée avec le cycle de l'eau de toute la région.

Industrie de pâte et papier
Surveillez la dureté totale dans les circuits d'alimentation en eau de l'usine pour vous prémunir contre la corrosion et/ou l'entartrage, ainsi que contre les effets d'une dureté élevée sur la qualité du produit.

Industrie des boissons
La dureté de l'eau utilisée pour préparer les boissons peut affecter leurs propriétés organoleptiques.

Comment mesure-t-on la dureté de l'eau ?


Titrage
La dureté est généralement mesurée par titrage colorimétrique avec une solution EDTA. Un titrage implique l'ajout d'un indicateur, puis de petites quantités de solution titrée à un échantillon d'eau jusqu'à ce que l'échantillon change de couleur. Vous pouvez titrer un échantillon pour évaluer sa dureté totale à l'aide d'une burette ou d'un kit de test. Vous pouvez également mesurer la dureté du calcium séparément de la dureté du magnésium en réglant le pH et en utilisant différents indicateurs.
Kits de test goutte à goutte
Ce test de dureté consiste à utiliser un compte-gouttes pour ajouter la solution EDTA à l'échantillon. Le nombre de gouttes est proportionnel à la dureté de l'eau. Le kit de test de dureté totale, modèle HA-71A, qui utilise l'indicateur ManVer, fonctionne mieux pour les échantillons d'eau naturelle, en particulier en présence de fer ou de manganèse, ou lorsque l'alcalinité est élevée. Les modèles de kits de test 5-B, 5-EP et 5-EP/MG-L, qui utilisent le réactif UniVer, fonctionnent mieux pour les échantillons industriels susceptibles de contenir de fortes concentrations de métaux, tels que le cuivre. D'autres kits de test sont disponibles pour mesurer séparément la dureté calcique et magnésienne.
Titrateur numérique
Les kits utilisant le titrateur numérique peuvent mesurer plus précisément la dureté que les kits de titrage goutte à goutte. En effet, le titrateur numérique distribue la solution EDTA en très petites quantités et avec une plus grande précision. Les kits de test de dureté avec titrateur numérique utilisent l'indicateur ManVer.
Dureté (totale et calcium), modèle HAC-DT
Dureté (séquentielle calcique et totale), kit de réactifs LR
Dureté (séquentielle calcique et totale), kit de réactifs HR

Bandelettes de test
Lorsque la bandelette de test de dureté de l'eau est plongée dans un échantillon d'eau, une couleur apparaît sur la bandelette et cette dernière est comparée à un tableau. Le tableau indique les couleurs pour les concentrations de 0, 25, 50, 120, 250 et 425 ppm, ou 1, 1,5, 3,7, 15 et 25 gpg. Utilisez les bandelettes de test lorsqu'une plage générale de dureté est suffisante. Les bandelettes de test ne doivent pas être utilisées lorsqu'une valeur de dureté exacte est requise.
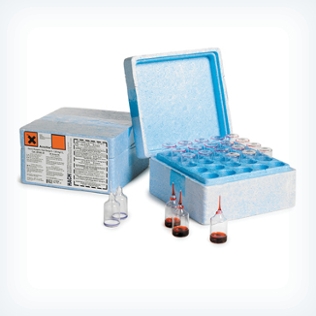
Colorimétrie ou spectrophotométrie
Utilisez un colorimètre ou un spectrophotomètre si vous devez mesurer la dureté d'une eau extrêmement douce, lorsque la concentration attendue est inférieure à 4 mg/L pour CaCO 3 (méthode à la calmagite).
Paillasse/portable :
Kit de réactifs pour la calmagite
Utilisez un spectrophotomètre si vous devez mesurer une très faible dureté dans l'eau, lorsque la concentration attendue est inférieure à 1 mg/L pour CaCO 3 (méthode par chlorophosphonazo).
Paillasse :
Kit de réactifs pour chlorophosphonazo, solution en vrac
Kit de réactifs pour chlorophosphonazo, sachets de solution
Utilisez un spectrophotomètre pour mesurer des plages plus élevées de dureté totale, Ca et Mg.
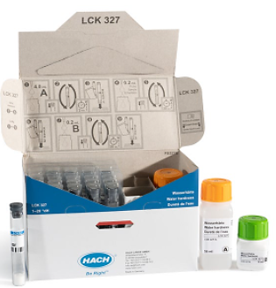

Electrode
Le calcium peut également être mesuré à l'aide d'une électrode sélective d'ions, telle que le modèle ISE25Ca Radiometer ou l'électrode sélective d'ions calcium (ISE) 9660C. L'électrode est la meilleure méthode à utiliser lorsque la couleur ou la turbidité de l'échantillon interfère avec le titrage colorimétrique ou les méthodes spectrophotométriques.
Paillasse :
Kit d'application de titrage pour l'eau AT1000 : dureté Ca et Mg (ISE)
Kit d'application de titrage pour l'eau AT1000 : pH/alcalinité et dureté (ISE)

Analyse en ligne
Les analyseurs en ligne permettent une surveillance continue de la dureté. Ces instruments peuvent activer des alarmes ou contrôler des pompes d'alimentation en produits chimiques lorsque la concentration de dureté atteint le niveau sélectionné.
Adoucissement de l'eau
Pour réduire la dureté indésirable, l'eau doit être adoucie. Les méthodes d'adoucissement se divisent généralement en deux grandes catégories :
Processus d'adoucissement par échange d'ions
Ce processus échange les cations responsables de la dureté par des cations n'agissant pas sur la dureté, généralement du sodium, à l'aide d'une matrice d'échange d'ions naturelle ou synthétique, par exemple de la résine. Les matrices naturelles incluent notamment le sable vert et la zéolite. Chaque résine (ou matrice) d'échange d'ions possède des propriétés différentes. Les matériaux synthétiques ont tendance à avoir une meilleure capacité d'échange, ils sont donc mieux adaptés pour éliminer les niveaux de dureté plus élevés. Les résines utilisant de l'hydrogène comme cation sont communément appelées déminéralisateurs et sont généralement composées de résines d'échange de cations et d'anions pour maintenir un pH neutre. Pour des raisons sanitaires, il est important de noter que la résine à base de sodium augmente les niveaux de sodium dans l'eau traitée. Cela peut également interférer avec certaines méthodes ULR de détermination de la dureté.
Une fois la capacité d'échange d'une résine épuisée, la majorité peut être régénérée. Il est donc important de surveiller la dureté de l'effluent afin de déterminer à quel moment la colonne doit être régénérée. Lors de ce processus en deux étapes, l'unité est d'abord rincée pour éliminer les sédiments, puis une saumure est diffusée à travers la résine, dans des conditions spécifiques, en vue de remplacer les ions calcium et magnésium accumulés par le cation utilisé à l'origine pour l'adoucissement.
Avantages
- Cette méthode n'affecte pas considérablement les autres propriétés de l'eau, telles que le pH.
- Outre le calcium et le magnésium, ce processus permet également d'éliminer d'autres cations responsables de la dureté.
- Ce processus peut permettre d'atteindre une dureté quasi nulle.
Inconvénients
- D'importants niveaux de fer ou de manganèse dans l'eau peuvent encrasser la résine d'échange d'ions.
- Les résines à base de sodium peuvent augmenter les niveaux de sodium dans l'eau traitée et interférer avec certaines méthodes ULR (plage ultra-basse) de surveillance de la dureté.
- Une forte teneur en matières solides peut encrasser les lits de résine et entraîner des dépenses supplémentaires.
Processus d'adoucissement par précipitation
Pour la précipitation, on utilise généralement le procédé à base de chaux sodée. Lorsque de la chaux est ajoutée à une eau dure, elle provoque une réaction avec la dureté carbonatée présente et produit des matières solides qui doivent ensuite être retirées de l'eau. La chaux et le carbonate de soude peuvent être utilisés ensemble pour éliminer la dureté carbonatée et non carbonatée. Par rapport à la précipitation du calcium, la précipitation du magnésium nécessite deux fois plus d'additif chimique et génère deux fois plus de boue à éliminer. L'excès de dioxyde de carbone doit être éliminé avant l'adoucissement, car il peut empêcher la précipitation à la chaux.
Avantages
- Ce processus peut éliminer l'excès de fer et de fluorure.
- En raison du pH élevé, ce processus peut éliminer les bactéries et les virus.
- Avec un contrôle approprié, cette méthode permet de maîtriser la corrosivité et l'entartrage.
Inconvénients
- Ce processus génère une quantité considérable de boue à éliminer.
- Les coûts d'exploitation et en produits chimiques sont élevés.
- L'ajout de carbonate de soude peut affecter les niveaux de sodium dans l'eau.
- La recarbonatation, ou la réintroduction de dioxyde de carbone, doit être effectuée après l'adoucissement visant à abaisser le pH, en vue d'éliminer l'excès de chaux et d'encourager la précipitation de tout le carbonate de calcium restant.
- Ce processus ne peut pas réduire la dureté à zéro.
- Ce processus requiert un haut niveau de compétence de l'opérateur.
Foire aux questions
Quelle est la différence entre la dureté et l'alcalinité ?
La dureté est la somme des ions métalliques plurivalents dans la solution, spécifiquement et majoritairement le calcium et le magnésium, tandis que l'alcalinité est une mesure de la capacité de la solution à neutraliser les acides (somme des ions hydroxyde, carbonate et bicarbonate). Dans les systèmes d'eau naturelle, le carbonate de calcium est habituellement présent et responsable des différentes caractéristiques de l'eau. La dureté et l'alcalinité sont exprimées sous forme de concentration de CaCO 3 pour faciliter la communication d'un seul nombre afin de représenter plusieurs produits chimiques et pour faciliter le calcul de la dureté carbonatée et non carbonatée d'une solution.
A quelle concentration de dureté considère-t-on qu'une solution est dure ou douce ?
Il n'existe aucun consensus universel quant aux concentrations exactes considérées comme dures ou douces. Les informations suivantes proviennent du ministère de l'Intérieur américain et de la Water Quality Association (d'autres organisations sont susceptibles d'utiliser des classifications légèrement différentes) :
|
Classification |
mg/L |
|
Douce |
0 à 17 |
|
Légèrement dure |
17 à 60 |
|
Moyennement dure |
60 à 120 |
|
Dure |
120 à 180 |
|
Très dure |
>180 |
Qu'est-ce que la dureté temporaire ou permanente ?
La dureté temporaire et la dureté permanente sont des termes utilisés pour différencier la dureté qui peut être éliminée en faisant bouillir l'eau (temporaire) de la dureté qui ne peut pas être éliminée par ébullition (permanente). La dureté temporaire est synonyme de dureté carbonatée. La dureté permanente est synonyme de dureté non carbonatée.
Comment calculer la dureté carbonatée et non carbonatée ?
La dureté carbonatée et la dureté non carbonatée peuvent uniquement être calculées si les valeurs de dureté totale et d'alcalinité totale sont connues :
|
Lien entre dureté et alcalinité |
Dureté non carbonatée, mg/L pour CaCO 3 |
Dureté carbonatée, mg/L pour CaCO 3 |
|
Dureté totale ≤ |
= Dureté totale |
0 |
|
Dureté totale ≥ |
= Alcalinité totale |
= Dureté totale - Alcalinité totale |